
[토요경제=김시우 기자] 대원제약이 유산균 제품 ‘장대원’의 FDA 등록을 승인으로 둔갑해 판매해온 것으로 드러나 논란이 불거졌다.
5일 아주경제에 따르면 대원제약은 2019년 미국 식품의약국(FDA)에 ‘장대원’을 일반의약품(OTC)으로 등록하고, 국내에서는 ‘FDA 승인’이라는 허위 표시로 광고 및 마케팅을 진행해왔다. 이를 통해 국내에서 2년간 50억원이 넘는 매출을 올린 것으로 알려졌다.
대원제약이 FDA에 등록한 제품은 △장대원 네이처 플러스 △장대원 프로바이오틱스 △장대원 프로바이오틱스 키즈 △장대원 네이처 키즈 등 총 4종이다.
일반의약품(OTC)의 FDA 등록은 임상실험 등이 필수가 아니다. 대원제약은 이 점을 이용해 등록을 마친 뒤 장대원을 2019년 3월 온·오프라인에서 ‘FDA 승인’ 제품이라며 마케팅을 전개했다는 것이다. 이는 허위·과장광고다.
국내에서 제조하는 일반의약품 및 건강기능식품은 미국에서 OTC로 분류할 수 있고, 전문의약품이나 신약 등에 비해 적은 비용과 간단한 절차로 FDA에 등록할 수 있다.
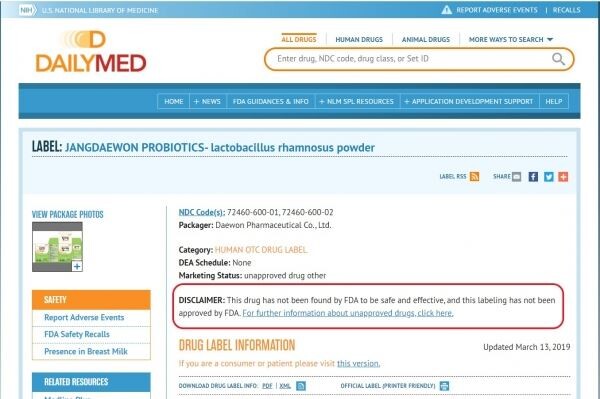
미국 국립의학도서관(NLM)이 운영하는 데일리메드는 장대원 4종에 대해 “안전하거나 효과가 있다고 FDA에 나타나지 않은 데다, FDA에서 승인된 명칭도 아니다”고 주의 문구를 사이트 내 장대원 소개 페이지에 첨부했다. 데일리메드는 미국 내 시판되는 약물에 대한 FDA의 정보를 제공하는 공공서비스다.
이에 백승열 대원제약 부회장 또한 논란을 책임져야 한다는 지적이 나오고 있다. 백 부회장은 FDA에 장대원이 등록하는 데 주도적인 역할을 한 것으로 알려졌다.
이번 사태로 공정경쟁을 지향하고자 노력하는 제약업계 신뢰를 무너뜨리고 불신을 가중시켰다는 지적에서 자유로울 수 없다는 것이 업계 지적이다.
식약처 관계자는 “FDA 등록과 승인은 엄연히 다른 말”이라며 “위반사항이 발견될 경우에는 제재를 받을 수 있다”고 말했다.
한편, 대원제약의 입장을 듣기 위해 연락을 시도했으나 닿지 않았다.
[저작권자ⓒ 토요경제. 무단전재-재배포 금지]





































